このシステムは医療機関等で実施される臨床研究について臨床研究法及び再生医療等の安全性の確保等に関する法律の規定に基づき 厚生労働大臣に対して実施計画の提出などの届出手続を行うためのシステムです また同法に規定する臨床研究実施基準に基づき世界保健. 平成27年3月 我が国における植込型補助人工心臓適応適正化に関するDestination Therapyについて補助人工心臓治療関連学会協議会植込型LVADの適応の適正化に関する検討ワーキンググルループ委員長 萩原誠久およびDestination TherapyDT研究会が中心となって検討を進めてまいりましたが今回.
Pmda Go Jp
Hsp Ehime U Ac Jp

医療機器製造販売申請の手引2019 公益財団法人 医療機器センター 本 通販 Amazon
日本医療検査科学会 第53回大会 2021年 10月8日金10日日 会場パシフィコ横浜 大会テーマ 日本医療検査科学会の未来を創る技術革新と人材育成 大会長 ごあいさつ 栁原 克紀 長崎大学大学院 病態解析診断学分野臨床検査医学教授 大会事務局 一般社団法人 日本医療検査科学会 旧.
新規医療機器認定 臨床期間. Pharmaceuticals and Medical Devices Agency は厚生労働省所管の独立行政法人である 医薬品機構 PMDA ぴーえむでぃーえーなどと略す. 日臨技臨床検査精度管理参加証 2021年度 pdf 及び 精度保証施設認証書_scc_2021-2023 pdf. 大分大学認定研究チームBURSTBundai Researcher Team 大分大学の研究グループ等で個別に行われている研究のうち独創的な研究異分野連携研究あるいは地域課題の解決を目指す実践的な研究などを行うグループを大分大学認定研究チームBURSTBundai Researcher Teamに認定し研究を.
医療機器規制関連セミナービデオ 180分で学ぶ医療機器ソフトウェア規制iec-62304要点セミナー 医療機器企業リスクマネジメントセミナー 180分で要点を学ぶ欧州医療機器規則mdrにおけるpmsビジランス対応要点セミナー. 2021年09月10日 2021年度第60回麻酔科専門医試験 試験会場への移動が困難である受験者への措置について.
医工連携特別インタビュー 医療機器の申請から承認までを 欧米並みの 14ヶ月 に
Pref Kyoto Jp

委員会について 研究倫理委員会 大阪医科大学 研究倫理委員会
Dbcentre2 Jmacct Med Or Jp
医工連携特別インタビュー 医療機器の申請から承認までを 欧米並みの 14ヶ月 に
Pmda Go Jp
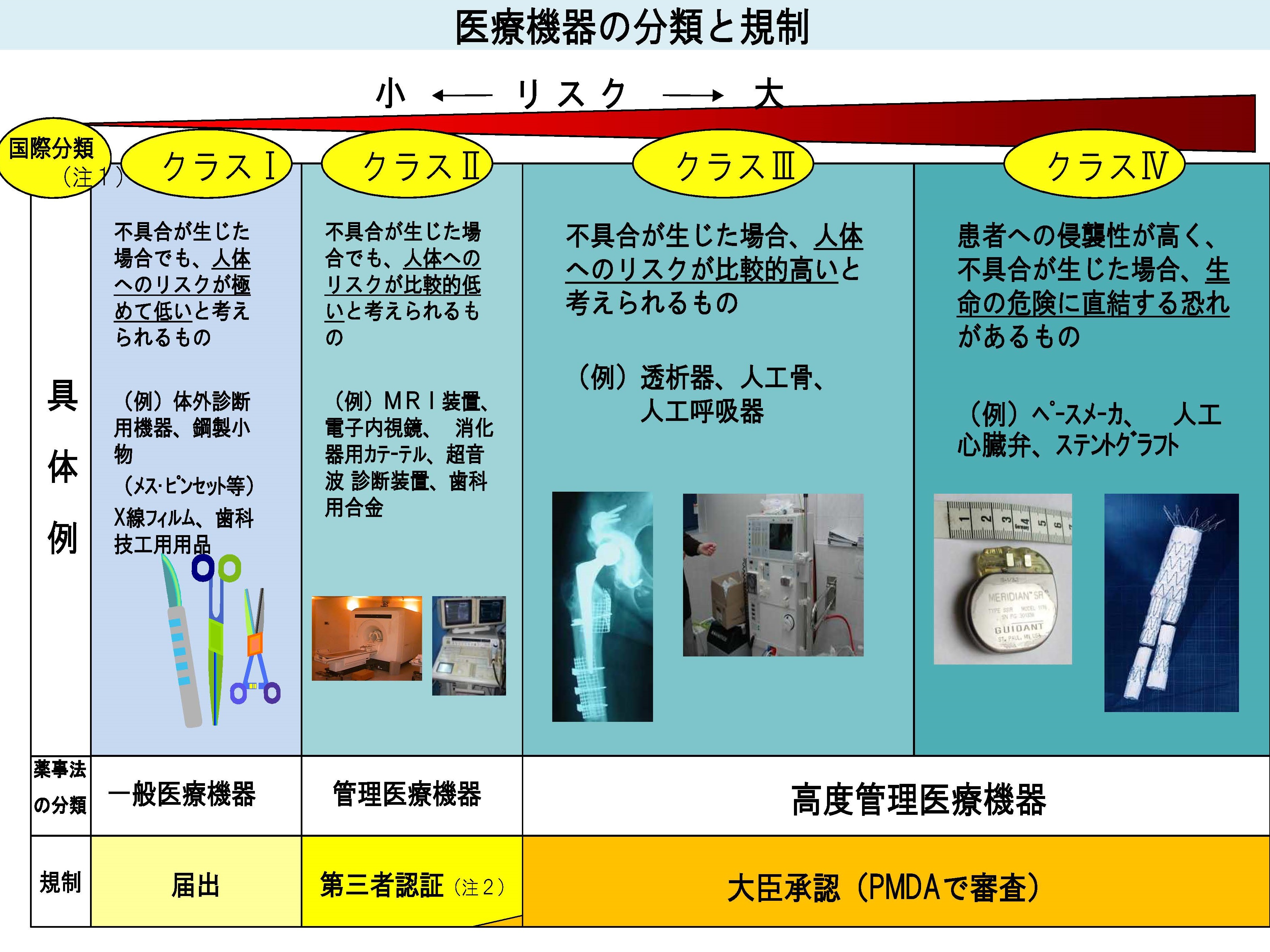
医療機器の分類を理解する Iso13485への対応ならワークシフト
/1667-tuv-r-visual-ivdr-en-draft02-jp_core_1_x.png)
Ivdr 体外診断用医療機器規則 Jp Tuv Rheinland
